Krebserzeugende Genfusionen fördern Entzündung und DNA-Schäden
durch spezielle RNA-Moleküle in Zellbläschen
Im Inneren jeder Zelle liegt der Bauplan unseres Körpers – die DNA. Sie besteht aus einer langen Kette von vier Bausteinen, die wie Buchstaben (A, C, G, T) unsere Erbinformationen speichern. Ausgewählte Abschnitte dieser DNA nennt man Gene – sie enthalten die Anleitungen zur Herstellung von Proteinen, also Eiweißen, die für nahezu alle lebenswichtigen Funktionen benötigt werden.
Damit ein Protein entstehen kann, wird zunächst eine Kopie des entsprechenden Gens in Form von RNA erstellt – dieser Vorgang heißt Transkription. Diese RNA-Kopie wandert aus dem Zellkern ins Zellinnere und dient dort als Vorlage, um das Protein zusammenzusetzen (Translation).
Wenn die Zellsteuerung aus dem Ruder läuft
Welche Gene wann aktiv sind, wird streng reguliert. Wichtige Schaltstellen dabei sind sogenannte Transkriptionsfaktoren – spezielle Proteine, die die Aktivität von Genen steuern. Eine besonders einflussreiche Gruppe dieser Faktoren ist die ETS-Familie. Bei vielen Krebsarten kommt es zu sogenannten Genfusionen, bei denen Teile zweier verschiedener Gene miteinander verschmelzen. So entstehen neue, veränderte Transkriptionsfaktoren, die die Zellsteuerung außer Kraft setzen können.
Solche Fusionen sind zum Beispiel typisch beim Ewing-Sarkom, einer seltenen, aber aggressiven Krebserkrankung bei Kindern und Jugendlichen. Zwei häufige Genfusionen dort heißen EWS:FLI1 und EWS:ERG. Ähnliche Veränderungen finden sich auch beim Prostatakrebs (z. B. TMPRSS2:ERG).
Unerwartete Aktivierung von „stiller“ DNA
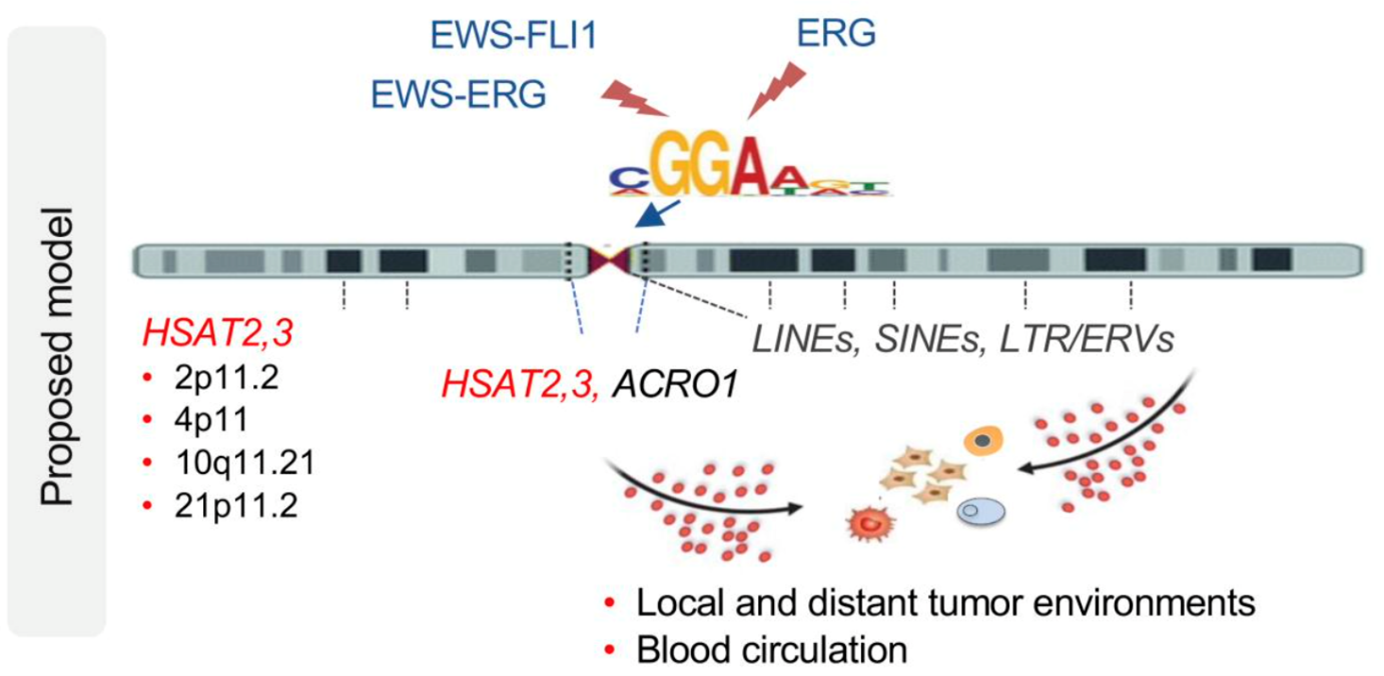
Ein internationales Forschungsteam unter Beteiligung von Peter Ruzanov und Valentina Evdokimova (Toronto, Kanada) hat nun herausgefunden: Diese veränderten Transkriptionsfaktoren können an bestimmte DNA-Stellen binden, die normalerweise stillgelegt sind – sogenannte repetitive Sequenzen rund um das Centromer, eine zentrale Stelle im Chromosom. Dort ist die DNA normalerweise dicht verpackt und nicht aktiv.
Trotzdem wird durch die ETS-Fusionen an diesen ungewöhnlichen Stellen RNA gebildet – insbesondere zwei Typen namens HSAT2 und HSAT3. Diese werden nicht in der Zelle behalten, sondern in kleinen Bläschen – extrazellulären Vesikeln (EVs) – verpackt und ins Blut abgegeben.
Kleine Bläschen mit großer Wirkung
Diese Vesikel verhalten sich wie winzige Pakete – oder wie Giftmüllpäckchen: Sie tragen problematische RNA-Moleküle in andere Zellen. Im Blut von Ewing-Sarkom-Patient:innen mit Metastasen finden sich besonders hohe Mengen davon.
In Laborversuchen zeigten die Forschenden: Wenn gesunde Bindegewebszellen (Fibroblasten) mit solchen EVs behandelt werden, kommt es zu DNA-Schäden und Zellalterung – also genau den Effekten, die auch für Krebs typisch sind. Die RNA aus den Vesikeln wirkt also fast „infektiös“. Zusätzlich lösen die RNA-Pakete eine chronische Entzündungsreaktion im Gewebe aus – ein Zustand, der die Streuung von Tumoren (Metastasierung) begünstigen kann.
Was bedeutet das für die Krebsmedizin?
Die Entdeckung, dass Tumorzellen ihre Umgebung durch RNA-haltige Vesikel beeinflussen können, öffnet neue Wege für Diagnose und Therapie:
- Die Menge an HSAT2- und HSAT3-RNA im Blut könnte als biomarker dienen, um das Fortschreiten einer Krebserkrankung besser zu überwachen.
- Gleichzeitig zeigt die Studie, wie eine seltene Krebserkrankung im Kindesalter – das Ewing-Sarkom – grundlegende Einblicke in biologische Mechanismen liefert, die auch bei häufigeren Krebsarten wie dem Prostatakarzinom eine Rolle spielen.
Ruzanov P, Evdokimova V, Pachva MC, Minkovich A, Zhang Z, Langman S, Gassmann H, Thiel U, Orlic-Milacic M, Zaidi SH, Peltekova V, Heisler LE, Sharma M, Cox ME, McKee TD, Zaidi M, Lapouble E, McPherson JD, Delattre O, Radvanyi L, Burdach SE, Stein LD, Sorensen PH. Oncogenic ETS fusions promote DNA damage and proinflammatory responses via pericentromeric RNAs in extracellular vesicles.
J Clin Invest. 2024 Mar 26; 134(9):e169470.
Copyright © 2025 American Society for Clinical Investigation
ISSN: 0021-9738 (print), 1558-8238 (online)
doi: 10.1172/JCI169470.
PMID: 38530366;
PMCID: PMC11060741.

